本文中の図やグラフは元論文より引用しております。
背景
- SAPHO(Synovitis-Acne-Pustulosis-Hyperstosis-Osteitis) 症候群は皮疹と、骨・関節症状が特徴的な疾患である
- 症状が多様であるため、Sterno-Costo- Clavicular Hyperostosis (SCCH) 、pustulotic arthro-osteitis (PAO) 、Chronic relapsing multifocal osteomyelitis(CRMO、小児に多い)とも呼ばれることがある
- 骨(骨過形成、骨炎)関節(滑膜炎)症状
- 主に前胸壁(胸鎖関節、胸骨柄結合、肋軟骨)、脊椎、仙腸関節が病変
- 四肢の小関節を病変とするのは稀
- 骨過形成
- 慢性の骨膜反応、皮質骨肥厚
- 骨炎
- 皮質骨、海綿骨の炎症
- 単発性 or 多発性
- 溶骨が骨硬化に先行することもある
- 皮膚症状
- 掌蹠膿疱症、重度のざ瘡、乾癬
- 1987年に、ChamotらがSAPHO症候群を提唱
- 診断基準
- 1988年にBenhamouらが以下を提唱
(Clin Exp Rheumatol.6(2):109-12,1988から引用)
診断項目
|
1 重度のざ瘡を伴う関節病変
2 掌蹠膿疱症(PPP)を伴う関節病変 3 四肢、脊椎、胸鎖・胸肋関節の骨肥厚症 4 体軸もしくは末梢の慢性再発性多発性骨髄炎(CRMO) |
判定
|
上記4項目中1項目を満たし、下記除外項目がない場合に診断される
|
除外項目
|
化膿性骨髄炎、感染による胸壁の関節炎、感染性掌蹠膿疱症、手掌角化症、びまん性特発性骨増殖症(DISH)、レイチノイド療法に伴う骨関節病変
|
- Kahnらの診断基準もある
- 以下のいずれかを満たす
- CRMO
- 急性、亜急性、慢性の関節炎+PPP、膿疱性乾癬、重度ざ瘡のいずれか
- 無菌性骨髄炎+PPP、膿疱性乾癬、尋常性乾癬、重度ざ瘡のいずれか
- Govoniら2003年ACRでのannual meetingで提唱したのは下
- これによれば骨病変が診断に不可欠
- 疫学
- SAPHO症候群の疫学は不明なことが多い
- ヨーロッパに多く(1/10,000人)、日本は比較的少ない(2.85/10,000,000人)
- 日本が少ないのは認知の問題かもしれず、SCCHやPAOに混ざっている可能性がある
- 海外では男性のほうが多いと報告もあるが、国内の報告では女性が多い
- 発症年齢は2峰性で、10-20歳台 & 50歳台
- CRMOは10歳代が多い
- SAPHO症候群の10-20歳台のピークはこれを反映しているのかもしれない
- HLA-B27との関連が以前言われていたほどより弱いことがわかり、脊椎関節炎との関連についても不明である
- pathogenesis
- 感染症、自己免疫、遺伝因子などがいわれている
- 鑑別診断
- 感染症、悪性腫瘍、骨Paget病、 Diffuse Idiopathic Skeletal Hyperostosis(DISH)など
- 骨病変のみの場合は鑑別が難しい
- 一般細菌、真菌、抗酸菌などが鑑別に上がる場合は骨生検が必要である
- 治療に関しても確立されたものはない
- NSAIDs、ステロイドなど
- Propionibacterium acnesに対する抗生剤が有効であることも報告されている
- 骨病変に関してはビスホスホネート製剤が有効
- 難治性の場合にはMTX生物学的製剤などのDMARDsが使用される
- 扁桃腺炎があればそれを治療するとPPPやSAPHO症候群の胸鎖関節病変が改善することも報告されている
- 予後
- 再燃と寛解を繰り返すが、長期的予後は比較的良好
日本からの67例のSAPHO症候群の報告(Hiroshi Okuno er al, Clinical features and radiological findings of 67
patients with SAPHO syndrome, Modern Rheumatology, 28 October 2017)
- 方法
- 東北大学で2002-2013年にBenhamouらの診断基準によってSAPHO症候群と診断された67例(44:女性、23:男性)を解析
- 結果
- 臨床所見(table1)
- 平均発症年齢:48.5歳
- 平均診断時年齢:53.1歳
- 併存症
- 扁桃腺炎
- 歯科疾患
- 副鼻腔炎
- 金属アレルギー
- 甲状腺炎
- 下痢・便秘
- 皮膚症状
- 皮膚症状の内訳
- 掌蹠膿疱症
- ざ瘡
- 乾癬
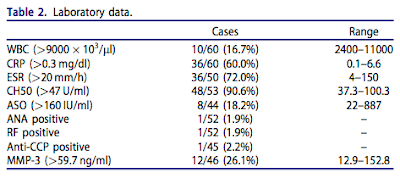
- 検査所見
- CRP、ESR増加:60-70%程度のみ
- WBC増加に関してはわずか16%
- RF、CCP抗体、ANA陽性:2%程度
- RF、CCP抗体陽性患者は右股関節痛の訴えがあったが、画像的には関節炎ではなく大腿骨の病変であり、ACR-EULAR 2010のRA分類基準も満たさなかった
- MMP-3増加:26%
- ASO増加:18%
- 骨生検
- 他疾患と鑑別目的で29.8%で施行
- いずれも一般細菌、真菌、抗酸菌は陰性
- 非特異的な炎症細胞浸潤もしくは慢性骨髄炎の所見を全例で認めた
- 画像所見
- X線(100%)、骨シンチ(46.3%)、CT(83.6%)、MRI(85.1%)を施行
- 以下の部位に所見が認められた
- 骨に所見あり:97%
- 前胸壁:77.6%
- 脊椎:41.8%
- 長管骨:14.9%
- 骨盤、顔面、肩甲骨:1.5%
- 手指骨:0%
- 関節に所見あり:46.2%
- 大関節(肩、股、膝、肘、足):13.4%
- 小関節(手、手指、足趾):4.5%
- 腱付着:13.4%
- 61歳女性
- X線(A):鎖骨の透過性低下
- CT(B):胸骨の骨過形成、胸鎖関節の強調
- 骨シンチ(C):胸鎖関節の集積亢進
- 26歳女性
- CT(A):終板の不整、椎間板狭小化、椎体辺縁のerosion
- MRI(B):T1強調画像での椎体領域の低信号、造影での不均質な取込み増加
- 25歳女性
- 大腿骨の骨膜肥厚
フランスからの41例の報告
(uhani, et al: The SAPHO syndrome. J Rheumatol 2015;42:329–34)
- characteristics(table1の一番右。他のシリーズとの比較)
- 前胸部疼痛が初発症状として多い
- 女性が多い
- 初発症状〜診断まで平均12ヶ月
- HLA-B27は測定された36例で全て陰性
- 治療
- コルヒチン
- 6例で使用されたがいずれも効果なし
- ステロイド内服
- 寛解まではいかないが症状改善
- SASP
- 6例で使用し、1人のみ関節病変改善、1人はPPPに著効
- MTX
- 4例に使用され、関節病変に対して10ヶ月時点で2例は無効、1例はわずかに有効、1例は有効だった
- 抗生剤
- アジスロマイシンで治療された7例において、1例ではgood response、1例ではpartial response、5例では無効
- ドキシサイクリンで治療された2例では、1例で無効、1例は副作用のため中止
- なお、この報告では反応性関節炎を除外しきれていない
- ビスホスホネート製剤
- パミドロン酸(180mg/回)で26例治療し、6ヶ月時点で22例が有効、疼痛に関しては17/22例で50%以上改善(100%改善が7/22例)
- TNF阻害剤
- IFX使用した1例では著効し3年間有効だった
- ETNで9ヶ月間治療しADAにスイッチした例ではいずれも無効だった
- 骨シンチでの左顎骨集積亢進
- 仙腸関節MRI、CT
- 左仙腸関節の前面に位置する軟部組織の炎症、左S1神経孔周囲の骨過形成
<SAPHOとRAの合併例>
Wenrui Xuらの報告(Medicine (2017) 96:1(e5724))
- 59歳、女性
- 2005年3月より両側PIP・手関節痛と朝のこわばりあり、RF・CCP抗体陽性(437 AU/mL)でRAと診断(table1)
- PSL 20mgで治療
- 2ヶ月後、症状安定しておりPSL10mg+LEF10mgへ変更し維持量として継続
- 2015年4月、腰痛、左胸鎖関節痛、掌蹠膿疱症が1ヶ月間で発症し、受診
- X線:腰椎に変性あり
- CT:左胸鎖関節の硬化性変化と皮質骨のerosionあり
- 血液検査:炎症反応増加(table1)
- 上記より、SAPHO症候群と診断されPSL15mgへ増量したが、2ヶ月後に皮膚症状・骨関節症状が再燃
- 骨シンチ:bull's head sign陽性
- tripterygium wilfordii polyglycosidium (TWP, 0.6g tid) +PSL15mgで治療開始し、症状は改善
- その後PSL中止した際に再燃し、PSL再開